Técnicas espectrofotométricas
-
Upload
rigoberto-jr-solis-martinez -
Category
Documents
-
view
2 -
download
0
description
Transcript of Técnicas espectrofotométricas

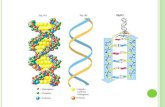
Técnicas espectrofotométricas:
Tipos de espectrofotometría:
Absorción de Infrarrojos Absorción de UV-Visible Resonancia magnética nuclear Fluorescencia Emisión atómica Absorción atómica de masas Fluorescencia de rayos X
Espectrofotometría Infrarrojo:
Espectroscopia infrarroja (Espectroscopia IR) es la rama de la espectroscopia que trata con la parte infrarroja del espectro electromagnético. Esta cubre un conjunto de técnicas, siendo la más común una forma de espectroscopia de absorción. Así como otras técnicas espectroscópicas, puede usarse para identificar un compuesto e investigar la composición de una muestra. Esta se puede dividir según el tipo de la radiación que se analiza, en:
Espectroscopia del Infrarrojo cercano Espectroscopia del infrarrojo medio Espectroscopia del infrarrojo lejano
Espectrofotometría UV-Visible:
La espectroscopia ultravioleta-visible o espectrofotometría ultravioleta-visible (UV/VIS) es una espectroscopia de emisión de fotones y una espectrofotometría. Utiliza radiación electromagnética (luz) de las regiones visible, ultravioleta cercana (UV) e infrarroja cercana (NIR) del espectro electromagnético, es decir, una longitud de onda entre 190nm y 780nm. La radiación absorbida por las moléculas desde esta región del espectro provoca transiciones electrónicas que pueden ser cuantificadas.
La espectroscopia UV-visible se utiliza para identificar algunos grupos funcionales de moléculas, y además, para determinar el contenido y fuerza de una sustancia.
Se utiliza de manera general en la determinación cuantitativa de los componentes de soluciones de iones de metales de transición y compuestos orgánicos altamente conjugados.
Se utiliza extensivamente en laboratorios de química y bioquímica para determinar pequeñas cantidades de cierta sustancia, como las trazas de metales en aleaciones o la concentración de cierto medicamento que puede llegar a ciertas partes del cuerpo.
Resonancia magnética nuclear:

La espectroscopía de resonancia magnética nuclear (RMN) es una técnica empleada principalmente en la elucidación de estructuras moleculares, aunque también se puede emplear con fines cuantitativos y en estudios cinéticos y termodinámicos.
Algunos núcleos atómicos sometidos a un campo magnético externo absorben radiación electromagnética en la región de las frecuencias de radio o radiofrecuencias. Como la frecuencia exacta de esta absorción depende del entorno de estos núcleos, se puede emplear para determinar la estructura de la molécula en donde se encuentran éstos.
La técnica se ha empleado en química orgánica, química inorgánica y bioquímica. La misma tecnología también ha terminado por extenderse a otros campos, por ejemplo en medicina, en donde se obtienen imágenes por resonancia magnética.
Fluorescencia:
La espectroscopia de fluorescencia, también llamada espectrofotometría o fluorimetría; es un tipo de espectroscopia electromagnética, la cual analiza la fluorescencia de una muestra. Esto involucra el uso de un haz de luz comúnmente de luz ultravioleta, que excita a los electrones en las moléculas de ciertos componentes y causa entonces la emisión de luz; típicamente, pero no necesariamente, luz visible. Su técnica complementaria es el espectro de absorción. El equipamiento que mide la fluorescencia es llamado fluorómetro o fluorímetro.
Emisión Atómica:
La espectroscopía de emisión atómica, en particular, es una técnica instrumental que tiene por objeto el estudio de la radiación procedente de los niveles electrónicos de los átomos después de que estos sean irradiados con una fuente de emisión.
La fuente de emisión por excelencia es la llama. En los primeros equipos, la muestra se añadía directamente a una llama producida en un mechero y se observaba su cambio de color. En la actualidad, la muestra emite cuando es excitada eléctrica o térmicamente como por ejemplo tubos de descarga de gases a baja presión, arco eléctrico y chispa. Otros elementos necesarios de los equipos son un sistema dispersivo y un detector.
Absorción atómica de masas:
La espectroscopia de absorción atómica (a menudo llamada espectroscopia AA o AAS, por Atomic absorption spectroscopy) es un método instrumental de la química analítica que permite medir las concentraciones específicas de un material en una mezcla y determinar una gran variedad de elementos. Esta técnica se utiliza para determinar la concentración de un elemento particular (el analito) en una muestra y puede determinar más de 70 elementos diferentes en solución o directamente en muestras sólidas utilizadas en farmacología, biofísica o investigación toxicológica.

La espectroscopía de absorción atómica fue utilizada por vez primera como una técnica analítica, y los principios subyacentes fueron establecidos en la segunda mitad del siglo XIX por Robert Wilhelm Bunsen y Gustav Robert Kirchhoff,, ambos profesores de la Universidad de Heidelberg, Alemania.
La forma moderna de la espectroscopia de absorción atómica fue desarrollada en gran parte durante la década de 1950 por un equipo de químicos australianos. Fueron dirigidos por sir Alan Walsh en la Commonwealth Scientific and Industrial Research Organisation (CSIRO), División de Química Física, en Melbourne, Australia.
Es un método de química analítica cuantificable que está basado en la atomización del analito en matriz líquida y que utiliza comúnmente un nebulizador pre-quemador (o cámara de nebulización) para crear una niebla de la muestra y un quemador con forma de ranura que da una llama con una longitud de trayecto más larga, en caso de que la transmisión de energía inicial al analito sea por el método "de llama". La niebla atómica es desolvatada y expuesta a una energía a una determinada longitud de onda emitida ya sea por la dicha llama, o una lámpara de cátodo hueco construida con el mismo analito a determinar o una Lámpara de Descarga de Electrones (EDL). Normalmente las curvas de calibración no cumplen la Ley de Beer-Lambert en su estricto rigor.
La temperatura de la llama es lo bastante alta para que la llama de por sí no mueran los átomos de la muestra de su estado fundamental. El nebulizador y la llama se usan para desolvatar y atomizar la muestra, pero la excitación de los átomos del analito es hecha por el uso de lámparas que brillan a través de la llama a diversas longitudes de onda para cada tipo de analito.
En AA la cantidad de luz absorbida después de pasar a través de la llama determina la cantidad de analito existente en la muestra. Hoy día se utiliza frecuentemente una mufla de grafito (u horno de grafito) para calentar la muestra a fin de desolvatarla y atomizarla, aumentando la sensibilidad.
El método del horno de grafito puede también analizar algunas muestras sólidas o semisólidas. Debido a su buena sensibilidad y selectividad, sigue siendo un método de análisis comúnmente usado para ciertos elementos traza en muestras acuosas (y otros líquidos). Otro método alternativo de atomización es el Generador de Hidruros.
Fluorescencia de rayos x:
La fluorescencia de rayos X (XRF, sigla en inglés) consiste en emisión de rayos X secundarios (o fluorescentes) característicos de un material que ha sido excitado al ser «bombardeado» con rayos X de alta energía o rayos gama. Este fenómeno es muy utilizado para análisis elemental y análisis químico, particularmente en la investigación de metales, vidrios, cerámicos y materiales de construcción, así como en la de geoquímica, ciencia forense y arqueología.

Los rayos X son un tipo de radiación electromagnética con una energía muy superior a la radiación ultravioleta que permite su absorción por los electrones de core. Los rayos X son especialmente capaces de penetrar estructuras cristalinas: su longitud de onda, de un orden de magnitud igual al de las distancias interatómicas.
Calibración de un espectrofotómetro:
1. Encender el espectrofotómetro.2. Esperar 15 minutos.3. Calibración: dependiendo del tipo de espectrofotómetro, algunos tienen la tecla
CAL para calibrar con un blanco; otros, por ejemplo, tienen la tecla Mode y están para elegir entre Absorbancia y transmitancia.
4. Seleccionar la longitud de onda, ya sea digitalmente o con una perilla analógica.5. Introducir la celda con el blanco con un volumen arriba de la mitad, pero no hasta
arriba, en el portaceldas del aparato. Presionar la tecla CAL y esperar a que la absorbancia se ponga a cero.
6. Hacer la curva de calibración con soluciones de concentración conocida.7. Después de hacer la curva es posible medir casi cualquier concentración de
cualquier muestra. :D
Reacción de formación del Ácido Acetilsalicílico:

No se encontraron datos termodinámicos para efectuar el requerimiento de energía de la reacción, pero es endergónica, eso lo sabemos.
El rendimiento de la reacción sucede en relación un mol a un mol. Por lo tanto, un mol de salicilato de metilo (138.12 g) producirán un mol de ácido acetilsalicílico (180.16 g). Tomando en cuenta que tenemos 4 gramos de ácido salicílico se espera obtener aproximadamente 5.22 gramos de ácido acetilsalicílico.
Partes principales de un espectrofotómetro:

Fuente de luz
La fuente de luz que ilumina la muestra debe cumplir con las siguientes condiciones: estabilidad, direccionabilidad, distribución de energía espectral continua y larga vida. Las fuentes empleadas son: lámpara de wolframio (también llamado tungsteno), lámpara de arco de xenón y lámpara de deuterio que es utilizada en los laboratorios atómicos.
Monocromador
El monocromador aísla las radiaciones de longitud de onda deseada que inciden o se reflejan desde el conjunto, se usa para obtener luz monocromática.
Está constituido por las rendijas de entrada y salida, colimadores y el elemento de dispersión. El colimador se ubica entre la rendija de entrada y salida. Es un lente que lleva el haz de luz que entra con una determinada longitud de onda hacia un prisma el cual separa todas las longitudes de onda de ese haz y la longitud deseada se dirige hacia otra lente que direcciona ese haz hacia la rendija de salida.
Compartimiento de Muestra
Es donde tiene lugar la interacción con la materia (debe producirse donde no haya absorción ni dispersión de las longitudes de onda). Es importante destacar, que durante este proceso, se aplica la ley de Lambert-Beer en su máxima expresión, con base en sus leyes de absorción, en lo que concierne al paso de la molécula de fundamental-excitado.
Detector
El detector, es quien detecta una radiación y a su vez lo deja en evidencia, para posterior estudio. Hay de dos tipos:
a) los que responden a fotones;
b) los que responden al calor.
Fotodetectores
En los instrumentos modernos se encuentra una serie de 16 fotodetectores para percibir la señal en forma simultánea en 16 longitudes de onda, cubriendo el espectro visible. Esto reduce el tiempo de medida, y minimiza las partes móviles del equipo.
Cubetas
Son los recipientes donde se depositan las muestras liquidas a analizar. Dependiendo de la longitud de onda a medir, serán hechas de cuarzo, vidrio o de material plástico. Se caracterizan por tener dos paredes correspondiente a los lados ópticos por donde cruza el haz de luz.
Diferencias entre colorímetro y espectrofotómetro:

Estos son equipos utilizados en el Laboratorio para el análisis de muestras fisiológicas, basándose en el principio que cada compuesto químico absorbe o emite energía lumínica de diferente longitud de onda. Esta longitud puede estar en el espectro de luz visible, o en otra parte del espectro electromagnético.
La diferencia fundamental entre un espectrofotómetro y un fotómetro o fotocolorímetro, consiste en que el fotocolorímetro trabaja únicamente en el espectro de luz visible y selecciona una longitud de onda determinada mediante filtros fijos.
En cambio, un Espectrofotómetro es capaz de trabajar, no solo con la luz visible sino que en otras regiones del espectro electromagnético (ultravioleta e infrarroja). Además posee un monocromador para seleccionar la longitud de onda deseada.
Tipos de lámparas utilizadas en espectrofotometría y su rango de uso:
Lámpara de filamento de tungsteno: Se utiliza para espectrofotometría visible y UV próximo. Su rango es entre 340 y 2500 nm aproximadamente.
Lámpara de filamentos de haluro de tungsteno: Emiten con más intensidad
Lámparas de hidrógeno y deuterio: Emiten para la región ultravioleta, van desde los 190 hasta incluso 800 nm.
Lámparas de vapor de mercurio: Sus emisiones características circulan entre 250nm, 300nm y 360nm. Se utilizan sobre todo en fluorescencia.
Diferencia entre Espectrofotometría UV y entre Visible:
La principal diferencia es el espectro de absorción y la lámpara utilizada, para UV se utiliza una lámpara de deuterio, mientras que para la visible se utiliza una lámpara de tungsteno. Muchos compuestos biológicos y farmacéuticos absorben en la región UV, por ejemplo las aspirinas, el DNA, las proteínas; mientras que compuestos como la urea absorben a aproximadamente 420 nm en el rango visible.
Rango de uso del espectrofotómetro Infrarrojo:

El rango de uso de los espectrofotómetros infrarrojos va desde los 780 nm hasta los 1,000,000 nm. Dependiendo si hablamos del infrarrojo cercano (780-2500 nm), infrarrojo medio (2500-15,400 nm) o del infrarrojo lejano (15,400-1,000,000 nm)
Diferencia entre UV e IR
Gracias a los IR podemos determinar la estructura y composición de una muestra, mientras que con el UV esto no es posible, también es posible con éste identificar compuestos y además cuantificarlos. Esas son las diferencias en aplicación, mientras que en instrumentación se necesitan distintas fuentes a las utilizadas en UV, por ejemplo bobinas de Nicromo, lámpara incandescente de Nernst, o el Globar.
Manejo del IR:
Encendido y calibración:
1. Quitar tapa de protección2. Mover rejilla de tal manera que no haya interferencia con el haz que se va a
proyectar3. Cerrar con la tapa de protección4. Encender el espectrofotómetro de IR5. Comenzar la rectificación de 60 segundos6. Observar si hay respuesta (sensibilidad)7. Observar en la pantalla si se marca una longitud de onda de 4000.
Colocación y lectura de la muestra
1. Quitar la tapa de protección2. Mover rejillas de tal manera que el haz incida sobre éstas3. Se coloca el portapastilla con todo y pastilla4. Establecer parámetros de ajuste (carta de expansión, tiempo de escaneado,
longitud de onda y la carta)5. Oprimir el botón de escaneado6. Finalizar lectura7. Leer el espectro.
Fuentes de radiación en IR:
Se puede utilizar una bobina de Nicromo de espirales muy juntas que se lleva a incandescencia por medio de un calentamiento resistivo. Se pueden lograr temperaturas de hasta 1100 °C. Esta fuente de radiación se recomienda cuando la confiabilidad es esencial. Aunque simple y resistente, esta fuente es menos intensa que otras.
La lámpara incandescente de Nernst es más caliente, y por tanto, más brillante, y permite una temperatura de operación que puede llegar hasta los 1500°C. Estas fuentes de

radiación se construyen con una mezcla fundida de óxidos de zirconio, itrio y torio, en cilindros huecos con 1-3 mm de diámetro y 2-5 cm de longitud. Las lámparas de Nernst son frágiles. La intensidad de la radiación es de aproximadamente el doble de las de nicromo o elementos Globar, excepto en el infrarrojo cercano.
El Globar, que es una varilla de carburo de silicio de 6-8 mm de diámetro y 50 mm de longitud, posee características intermedias entre los alambres calentados y la lámpara de Nernst. No es necesario calentarlo previamente y tiene una temperatura de operación cercana a los 1300°C
Los arcos de mercurio de alta presión con un recubrimiento extra de cuarzo para reducir pérdidas térmicas proporcionan radiaciones intensas en el infrarrojo muy lejano.
Tipos de detectores para IR:
Hasta los 1200 nm los métodos de detección usuales son iguales a los empleados para UV o visible.
Los detectores que se usan en las longitudes de onda más largas se clasifican en dos grupos más generales:
Detectores térmicos: en los que la radiación infrarroja produce un efecto de calentamiento que modifica alguna propiedad física del detector, los más comunes son: termopar, termisor, detector piroeléctrico.
Detectores Fotónicos: Que usan los efectos cuánticos de la radiación infrarroja para cambiar las propiedades eléctricas de un semiconductor, algunos de los más comunes son: Detector fotovoltaico y fotoconductor.
Diferencia entre fosforescencia y fluorescencia:

El mecanismo físico que rige este comportamiento es el mismo que para la fluorescencia, no obstante la principal diferencia con ésta es que hay un retraso temporal entre la absorción y la reemisión de los fotones de energía. En la fosforescencia, las sustancias continúan emitiendo luz durante un tiempo mucho más prolongado, aun después del corte del estímulo que la provoca, ya que la energía absorbida se libera lenta (incluso muchas horas después) y continuamente.
Componentes básicos de un fluorómetro y sus funciones:
En la espectrometría de fluorescencia se utilizan dos tipos generales de instrumentos:
Fluorómetros de filtro. Utilizan filtros para aislar la luz incidente y la luz fluorescente.
Espectrofluorómetros. Usan monocromadores de retículo de difracción para aislar la luz incidente y la luz fluorescente.
Ambos tipos de instrumentos utilizan el siguiente esquema. La luz de una fuente de excitación pasa a través de un filtro o monocromador, e incide sobre la muestra. Una parte de la luz incidente es absorbida por la muestra, y algunas de las moléculas de la muestra producen una fluorescencia. La luz fluorescente es emitida en todas las direcciones. Parte de esta luz fluorescente pasa a través de un segundo filtro o monocromador y llega a un detector, el cual muy a menudo se encuentra a 90° con respecto al haz de luz incidente para minimizar el riesgo de que la luz incidente reflejada o transmitida llegue al detector.
Diversas fuentes de luz pueden ser utilizadas como fuentes de excitación, incluyendo el láser, fotodiodos y lámparas; arcos de xenón y lámparas de vapor de mercurio. Un láser sólo emite luz de alta irradiancia en un intervalo muy estrecho de longitudes de onda, por lo general a 0,01 nm, lo que hace innecesario el monocromador de excitación o el filtro. La desventaja de este método es que la longitud de onda de un láser no se puede cambiar mucho. Una lámpara de vapor de mercurio es una lámpara lineal, lo que significa que emite luz cerca del pico de longitudes de onda. Por el contrario, un arco de xenón tiene un espectro de emisión continuo con intensidad casi constante en el rango de 300-800 nm, y una irradiancia suficiente para las mediciones hasta justo por encima de 200 nm.
En los fluorímetros pueden usarse filtros y/o monocromadores. Un monocromador transmite luz de una longitud de onda y tolerancia ajustables. El tipo más común de monocromador utiliza un retículo de difracción; es decir, la luz colimada entra en una rejilla y sale con un ángulo diferente dependiendo de la longitud de onda. El monocromador puede entonces seleccionar qué longitudes de onda transmite. Para

permitir mediciones de anisotropía se añaden dos filtros de polarización: uno después del monocromador de excitación o filtro, y otro antes del monocromador de emisión o filtro.
Como se mencionó antes, la fluorescencia se mide más a menudo en un ángulo de 90° en relación a la luz de excitación. Esta geometría se utiliza en lugar de colocar el sensor en la línea de la luz de excitación en un ángulo de 180° a fin de evitar la interferencia de la luz de excitación transmitida. El monocromador no es perfecto y transmitirá la luz con otras longitudes de onda diferentes a las establecidas. Un monocromador ideal sólo transmite luz en el rango especificado y tiene una transmisión independiente de la longitud de onda. Al medir en un ángulo de 90º, sólo la luz dispersa por la muestra provoca luz. Esto se traduce en una mejor relación señal-ruido, y reduce el límite de detección a un factor de aproximadamente 10000, si se compara con la geometría de 180°. Por otra parte, la fluorescencia también puede ser medida desde la parte delantera, procedimiento que se utiliza a menudo para las muestras turbias.
El detector puede ser de un solo canal o de múltiples canales. El detector de un único canal sólo puede detectar la intensidad de una longitud de onda en cada momento, mientras que el de múltiples canales detecta la intensidad en todas las longitudes de onda simultáneamente, con lo que el monocromador de emisión o filtro es innecesario. Los diferentes tipos de detectores tienen sus ventajas y desventajas.
El fluorímetro más versátil, con monocromadores dobles y una fuente de luz de excitación continua, puede registrar tanto un espectro de excitación como un espectro de fluorescencia. Al medir los espectros de fluorescencia, la longitud de onda de la luz de excitación se mantiene constante, de preferencia en una longitud de onda de alta absorción, y el monocromador de emisión escanea el espectro. Para medir los espectros de excitación, la longitud de onda que pasa a través del filtro o monocromador de emisión se mantiene constante y el monocromador de excitación va escaneando. El espectro de excitación generalmente es idéntico.
Aplicación industrial de la fluorimetría:
La espectrometría de fluorescencia se utiliza en análisis bioquímicos, médicos, químicos y de investigación de compuestos orgánicos. También se ha utilizado para diferenciar los tumores malignos de piel de los benignos.
La fluorescencia también puede utilizarse para reorientar los fotones.

Rangos de longitud de ondaen donde se puede realizar la medición:
El rango de trabajo es desde los 200 hasta los casi 500 nm, dependiendo de la sustancia a analizar se necesitará una longitud de onda adecuada para excitar el material fluorescente y hacer que éste emita luz a una longitud diferente.

300 350 400 450 500 550 600 6500
0.2
0.4
0.6
0.8
1
1.2
1.4
1.6
1.8Rangos de absorción de 50 en 50 nm
Longitud de onda
Abso
rció
n Abs. Máx. a 400 nm

385 390 395 400 405 410 415 4201.46
1.48
1.5
1.52
1.54
1.56
1.58Absorción óptima para la leer muestra
Longitud de onda
Abso
rban
cia Abs. Máx.
a 410 nm

0 0.5 1 1.5 2 2.5 3 3.51.36
1.365
1.37
1.375
1.38
1.385
1.39
1.395Curva de calibración con referencia (salió mal)
Concentración en mg
Abso
rban
cia

Rango de uso del refractómetro:
El refractómetro generalmente tiene una escala graduada en la que se mide el índice de refracción, en la mayoría de los refractómetros la escala para el índice de refracción es de 1.30 a 1.74
Manejo del refractómetro:
Ajuste de la escala
1. Colocar de 2 a 3 gotas de agua destilada en la superficie del prisma principal con una jeringa. (figura 3)
2. Cierre el prisma secundario y observa a través del ocular.
3. Ajusta la escala, a 1.333 ( Brix 0%). (figura 4)

B.- Medición del índice de refracción de las soluciones
1.- Abriendo el prisma secundario coloca de 2 a 3 gotas de solución en el centro de la superficie del prisma 2.- Cierra cuidadosamente el prisma secundario
3.- Observa por el ocular, gira la perilla de compensación de color hasta que aparezca una línea clara y definida en el campo de visión
4.- Gira la perilla de medición alineando la línea delimitadora con las líneas de intersección
5.- Leer en la escala superior el índice de refracción
Tipos de refractómetros:
Refractómetro de Abbe

Refractómetro de Abbe. Modelo antiguo
El refractómetro de Abbe permite obtener una medición del índice de refracción de un líquido depositándolo sobre una superficie de vidrio, colocándolo en un dispositivo óptico, y ajustando un botón para conducir una placa iluminada hacia el centro de un retículo.
Refractómetro de ángulo variable
El líquido se encuentra en una cubeta cuyo fondo es de hoja paralela. Esta hoja es iluminada en incidencia rasante por debajo. Todo tiene lugar como si el líquido fuese iluminado en incidencia rasante desde el aire. Un visor recupera el rayo y determina su ángulo.
Refractómetro de inmersión
El refractómetro se sumerge en el líquido a analizar. Sólo posee un único prisma, equivalente al prisma inferior de la descripción anterior de refractómetro de Abbe. No existe posibilidad de reflexión parásita, el rayo emergente es más preciso y un engrosamiento más fuerte es entonces posible. He aquí el interés de este dispositivo. Permite por tanto obtener una décima más que para el refractómetro de Abbe (4 unidades del quinto decimal). La iluminación se realiza a través de un espejo.
El refractómetro de inmersión permite dosificar los solubles disueltos en el agua, de débiles variaciones de índice precisamente conocidas. Es mencionado para análisis agroalimentarios.3 A consecuencia del engrosamiento considerable, un débil rango de índice solamente es accesible: entre 1,325 y 1,367.1
La extremidad del refractómetro a inmersión está directamente sumergida en el líquido, como un termómetro, y una anilla permite acromatizar la medición. Es necesario pues

disponer de una mayor cantidad de muestra que con el refractómetro de Abbe, lo que no plantea generalmente problemas con las soluciones acuosas.
Refractómetro portátil
Para medir los índices de refracción del jugo de las frutas sobre el terreno existen refractómetros portátiles. Funcionan sin alimentación, directamente con la luz natural. Estos instrumentos son calibrados de tal manera que indican 0 para el agua destilada, y directamente la concentración en azúcar de los jugos de las frutas analizadas. El jugo a analizar se deposita sobre el prisma, se cierra la tapa y el instrumento se dirige hacia la luz. Basta entonces con realizar una lectura directa. Una compensación automática de temperatura permite eliminar la variación de este factor, corriente sobre el terreno. La compensación es de 0,00045 unidades de índice de refracción por grado celsius alrededor de 20°C.4
Existen asimismo refractómetros digitales modernos que funcionan de forma automática y muestran el resultado en una pantalla. Este es más preciso y menos propenso a fallos humanos que una medición manual. Los resultados pueden ser transferidos directamente para la elaboración automática a un ordenador o una red a través de un interfaz estándar.