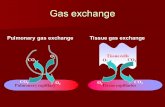
Model based gas exchange monitoring
-
Upload
cosmin -
Category
Health & Medicine
-
view
73 -
download
1
description
Transcript of Model based gas exchange monitoring

Principii de ventilatie mecanica
in ALI/ARDS
2010
SUUB

ALI/ARDS - definitie NAECC – North-American European Consensus Conference 1994
Sindrom caracterizat prin inflamatie
pulmonara acuta si persistenta,
permeabilitate vasculara si alveolara
crescuta .
( Bernard et al AJRCCM)

ALI/ARDS – definitie NAECC
• debut acut
• infiltrate pulmonare bilaterale (RxCP)
• PaO2/FiO2 = 201- 300 mmHg
PaO2/FiO2 ≤ 200 mmHg
• PAWP ≤ 18 mmHg sau/si fara dovada
clinica de LAH
( Bernard et al AJRCCM)

SINDROMUL este heterogen prin
definitie
• usor de aplicat in practica
• reproductibil - intre observatori
- independent de timp/tratament (pe
un interval mic de timp )
• valid - in acord cu un gold standard
- identifica pacienti cu prognostic similar (?
vezi STEMI anterior vs inferior, ambele SCA)
- identifica pacienti care raspund la un
tratament specific

• revarsate pleurale
• volume pulmonare mici
• variabilitate intre observatori
• dezacord cu examen CT
Rx
• variabil cu FiO2, PEEP, Paw
• dependent de frecventa de recoltare EAB
• nu reprezinta suntul la FiO2<0,8 IH
• exclude pacientii cu ALI + EP
• variabilitate interobservatori
• PAWP este dependenta de Pintratoracica
• nu exista un protocol clinic pentru LAH LAH
Dupa Rubenfeld

0
10
20
30
40
50
60
70
80
NAECC
DAD
Pneumonie
Edem
Altele
NAECC 1994 vs DAD
DAD-Gold Standard
Esteban et al, Ann Intern Med 2004

NAECC 1994
NAECC
OBEZ+BPOC
ARDS ALI

NAECC 1994
• Barbat, 38 ani,
victima accident rutier,
politraumatism,
contuzie pulmonara bilaterala, ruptura
splenica, hemoragie
retroperitoneala,
pancreatita acuta
postraumatica.
• 6 unitati MER, 8
unitati PPC , 14 unitati
CPP
• IH= 120 la FiO2= 0,7

ALI / ARDS – Diagnostic diferential:
• EP cardiogen
• DAH
• Pneumonia acuta eozinofilica idiopatica
• Pneumonia lupica
• Proteinoza alveolara
• Infiltrat leucemic
• Sarcoidoza
• Pneumonia acuta
interstitiala (Hamman-Rich)
• Clinica
• Istoric
• Eco
• BNP
• Swan Ganz
• Bronhoscopie
• Biopsie
• CT
www.uptodate.com

PaO2/FiO2 si rude indepartate
sau MIGET la patul bolnavului
paO2/
FiO2
VDphys
VDalv
Sunt+
V/Q mism
Sunt+
VDalv Rdiff
Sunt+
Rdiff
V/Q
mism sunt
GEP

SPATIUL MORT ALVEOLAR

Spatiul mort alveolar - de ieri si pana azi-
Bohr– fol.pt.a prezice un PACO2
- VD anat.estimat pe cadavre
-in prezent-fie PAC02=EtCO2=>VD anat
Enghoff modif.(1938)
Alveolar dead space
PACO2-alv mixed-
EtCO2(mean)
EtCO2=mean!-
(min+max)/2
alv

Spatiul mort alveolar
• este dependent de sunt ( “shunt dead space” –
Suter,1975)
• PaCO2 > PACO2 astfel ca va supraestima
adevaratul spatiu mort
• separare precara intre regiuni cu VA/Q si cele
cu VA/Q = ∞(spatiul mort “adevarat”) (
solubilitate CO2 modesta ≠ acetona – foarte
solubila, folosita in MIGET, VD repr. de
VA/Q>100)
• V/Q mismatch => “sloping alveolar plateau” • Uneori PetCO2 > PaCO2

Spatiul mort alveolar - dependenta de sunt (venous admixture) -

Spatiul mort alveolar
- ∆ CO2 negativ -
Spatiu mort alveolar mic dar ↑/Q mismatch

Spatiul mort alveolar
- ∆ CO2 negativ -
↑/Q mismatch

Spatiul mort alveolar
- ∆ CO2 negativ -
PCO2 alveolar variaza cu I/E, fiind maxim la sfarsitul expirului si minim la
sfarsitul inspirului.EtCO2 este un “varf” alveolar regional si temporal iar
PaCO2 este o “medie “ alveolara multiregionala (complet regionala) si temporala.Conditii cu FRC mic si VCO2 mare , mismatch crescut predispun
la ∆CO2 negativ.

Spatiul mort alveolar
- ∆ CO2 negativ -
Rezultatul a 2 compartimente diferite – slow si fast. Fast – golire initiala rapida; asta
presupune un FeCO2 relativ constant, deci un sloping de faza 3 initial minim . In paralel ,
slow – golire constanta, producand un sloping moderat de faza 3, initial dar si final. Fast
(spre final) – flow expirator mic , volum alveolar “restant, post golire initiala” mic si VCO2
constant crescut–toate sunt responsabile de un FeCO2fast crescut (upswing sau faza IV ).
Aceasta faza IV este diferita de faza IV de la SBA N2!
Ex. Pacientii obezi cu Etoracica mare ~model “fast”

Spatiul mort alveolar -CLINIC-
PULMONARY DEAD-SPACE FRACTION AS A RISK FACTOR FOR DEATH IN THE ACUTE RESPIRATORY DISTRESS SYNDROME - THOMAS J. NUCKTON

Spatiul mort alveolar -CLINIC-
Optimum End Expiratory Airway Pressure in Patients with Acute Pulmonary Failure – Suter PM, NEJM1975
Cel mai bun
PEEP corespunde
celei mai mici fractii
a spatiului mort si
celei mai bune
compliante

Spatiul mort alveolar -CLINIC-
Compliance and Dead Space Fraction Indicate an Optimal Level of Positive End-Expiratory Pressure After Recruitment in Anesthetized Patients - Stefan Maisch

Spatiul mort alveolar - CLINIC –
CAPNOGRAMA VOLUMETRICA
β

Spatiul mort alveolar - CLINIC –
Fazele capnogramei volumetrice
Faza 1 – cuprinde Vdaw ( o parte )
– mijlocul fazei 2 reprezinta limita Vdaw
– gaz alveolar = interfata dintre convectie si
difuzie ; contine cealalta parte din Vdaw si o
parte din gazul alveolar
- poate fi influentata de τ; daca ∆τ 0 => β (panta fazei 2) = > ventilatie omogena
– gazul alveolar
- panta e influentata de V/Q ; daca
∆↑/Q 0 atunci α (panta se “apleaca”) – VT CO2
FAZA 1
FAZA 2
FAZA 3
ARIA

Spatiul mort alveolar - CLINIC –
CAPNOGRAMA TEMPORALA VS. VOLUMETRICA
AVANTAJE
simpla
monitorizare pacienti
neintubati
monitorizeaza
expirul dar si inspirul
DEZAVANTAJE
nu reflecta V/Q ( un volum mai mic de gaze expirate ≈ 15%(la final) ocupa jumatate
din timpul de expir astfel ca un acelasi ∆ FCO2 ( comp. cu CV ) este distribuit pe o
“distanta” mai mare, deci α , adica panta fazei 3 este
“fals aplecata”) nu poate fi folosita pentru
estimarea componentelor VT

Spatiul mort alveolar - CLINIC -
VD
FOWLER≈
DRAGER
FLETCHER≈
NICO
TANG

Spatiul mort alveolar - CLINIC –
FOWLER 1948
Fowler Dead Space
equals
Anatomic Dead Space

FOWLER
• Ay=ABCD=PNCD
• AMP=MNB=Ax
• Ay=VTCO2
• PNCD=PD×(PN+CD)/2=VTPD×meanCO2alv
• VTCO2=mean expCO2×VT=mean expCO2(VTPD + VTOP)
• ( VT – VTOP) × mean CO2alv= mean expCO2×VT
• VTOP/VT= (meanCO2alv-mean expCO2 )/meanCO2alv
D
o

Spatiul mort alveolar - CLINIC –
DRAGER
Yearbook 2006
RASPUNS
With our CO2 measurement we are measuring the sum of the physiological death space and the anatomical death space.
Vds = Vdanatomic×2+Vdalv

Spatiul mort alveolar -CLINIC-
FLETCHER 1981
X = VT alv
Z =
VD anat
Y = VD alv

Spatiul mort alveolar -CLINIC-
FLETCHER 1981
Z
Y
X

FLETCHER
• Az/Axyz=PaCO2×VDanat/PaCO2×VT=VDanat/VT
• Ax=VTCO2=EtCO2mean×VTalv
• Ay=VTalv×( PaCO2-meanEtCO2 )
• VTalv×meanEtCO2=VTalveficient×PaCO2
• Ay=VTalv×PaCO2 – VTalveficient×PaCO2
• Ay=PaCO2×VDalv=>Ay/Axyz=VDalv/VT
• (Ay+Az)/Axyz=VDphys/VT

Spatiul mort alveolar - CLINIC –
TANG 2006

Spatiul mort alveolar - CLINIC –
TANG 2006
VD anatomic si VD fiziologic pot fi citite direct de pe abscisa

Spatiul mort alveolar - CLINIC –
TANG 2006
VD anatomic si VD fiziologic pot fi citite direct de pe abscisa
=225 ml
=160 ml
=65 ml

TANG
• Fie AOJA = AHJI (Fowler) si AOKB = AFEDK (Tang)
• VT = OC ; VDanat = OA(Fowler) ; VDphys = OB (Tang)
• PECO2 = AODC /VT
• VDphys Enghoff = VT×(1-PECO2/PaCO2) =
= VT×(1-AODC/ (PaCO2×VT))
• AODC = AOKB + ABKDC = ABKDC+AFEDK = ABCEF
• VDphys Enghoff = VT×(1-ABCEF/(PaCO2×VT) =
= VT×(1-(PaCO2×BC)/(PaCO2×VT)) = OB = VDphys Tang
G F E
D
H
I
K
J
C
J
A B C
D
E F G
H
I
K

Spatiul mort alveolar - CLINIC –
Recrutabilitate
Recrutarea impinge curba la stanga

Spatiul mort alveolar - CLINIC –
Recrutabilitate
Schimb gazos +
panta faza 3
aria
↑Dalv
Pa-ETCO2
Transp.gazos intraacinar +
panta faza3
panta faza2
vol III
VD phys
VD aw
VD alv
VD phys/VT

Spatiul mort alveolar
• titrarea PEEP-ului
• lung protective ventilation
Further studies needed....

Rdiff – limitarea difuziei

Suntul ( venous admixture )

Suntul ( venous admixture )
CcO2-CaO2/
CcO2-Cv02
True shunt(S1)
La FiO2=1,ai S2>S1 prin
atelect.de res.
V/Q mismatch

V/Q mismatch

Am vorbit despre...
Modele monopa-rametrice
V/Q mismatch
Spatiul mort
alveolar Rdiff
Sunt

“Fitting”-ul modelelor monoparametrice
4 valori SaO2/FeO2 pentru acelasi pacient
suntul si fA2 determinate pentru fiecare din cele 4 situatii
2 curbe – “fitting”-ul modelelor la datele pacientului
linia punctata – reprezinta curba pentru Rdiff, VD, V/Q
mis ( “fit” similar )
linia continua – reprezinta curba pentru sunt

“Fitting”-ul modelelor monoparametrice
insuficiente in a descrie schimburile gazoase
dependente de FiO2
Vd poate fi un marker pentru prognostic
Vd, suntul ( “state of art” ) – des folosite in a
urmari un ALI/ARDS – sunt insuficiente pentru
acest scop

Solutia este....
Modele biparametrice

Modele biparametrice
Shunt ∆PO2
∆=Pmixed alv-
Pcapilar unmixed

Modele biparametrice
• Rdiff(∆PO2) Shunt
• AlveolarDS(∆PO2) Shunt
• ↑/Q mismatch(∆PO2) Shunt

Modele biparametrice
Shunt + Rdiff
Shunt + VD
Shunt + V/Q
mismatch

Modele biparametrice Shunt + V/Q mismatch
Ventilatie
Conservarea masei O2-comp.alv
Conservarea masei O2 - sange
Continutul in O2 - sange
• Q1/Q2= 1/9 • fA2=VA2/VA=0,9->OPTIM • ∆PO2=PAO2-PcO2 • ∆PO2 NU depinde de fA2
=

Modele biparametrice
Fitting
Shunt=7,5%
∆PO2=6kPa=45mmHG
Modelul shunt/Vdalv-nepotrivit pt.masurarea Vdalveolar efectiv
Rdiff, Vdalv, V/Q mismatch sunt toate 3 “imaginea” ∆PO2
∆PO2 este “tradus” in Rdiff, Vdalv,V/Q mismatch laolalta

Modele biparametrice
-simulare shunt /fA2(∆PO2)-
∆PO2=0,variatie a shuntului pana
la 35%, “trage” curba vertical, in jos
Shunt=0,variatie a imaginii “∆PO2”’-fA2, “trage” curba la dreapta

Modele biparametrice
-susceptibilitate la hO2-
• Variatie FeO2 de la ≈0,25 la ≈0,18. Risc de hO2
mai mare pentru cazul 3. • ∆PO2 aduce risc de hO2 mai mare ca shunt la
aceeasi SaO2.

Modele biparametrice
-clinic-
Shunt
∆PO2
RECRUTABILITATE
∆PO2↑
-permeab.alv-capil.
-P hidrost
WET LUNG
Shunt↑
- atelectazie
-condensare
-supradistensie si shunt prin
cap.extralveol

Modele biparametrice -ALPE sau MIGET la marginea patului in 10-15 min-
• Ventilator ( Servo 300, 900 Siemens, Sweden )
• Analizor gaze ( FiO2, FeO2, FiCO2, FeCO2 ) – Datex AS-3, Datex- Engstrom,
Helsinki , Finland • Pulsoximetru
• Computer

Modele biparametrice -ALPE sau MIGET la marginea patului in 10-15 min-
De la rosu la albastru sau dupa “uscarea “ plamanului


ALPE

ALPE

Promisiune...

Hall of Fame
Stewart-
Strong Ion
Calculator
LUFU
Weissman
INVENT
Rees
Engstrom
Stenqvist
ALPE
Kjaergaard
Otis/Mead
Hamilton
Radiometer
Siggaard-
Andersen
Kellman

Indicele de hipoxemie PaO2/FiO2
inclus in NAECC si LIS
Imagine insuficienta a shuntului
nu este un parametru “independent” relatie nonlineara intre FiO2 si PaO2/FiO2
dependenta de shunt, AVD, PaCO2, RQ, Hb
(la aceeasi parametri ventilatori)

• AVD = constant (DC=constant->metabolism constant )
• S – variaza
• IH variaza cu FiO2 la acelasi shunt
Indicele de hipoxemie PaO2/FiO2
- variabilitate -

• AVD = variaza ( DC=constant -> ∆ metabolism)
• S – constant
• IH variaza fct.de AVD in conditiile unui sunt constant ( inv.prop.cu AVD )
Indicele de hipoxemie PaO2/FiO2
- variabilitate -

Indicele de hipoxemie PaO2/FiO2
- variabilitate -
• simulare model shunt=0-30% , ∆ pO2=0
• linii ingrosate – SaO2 relevante clinic ( 92 – 98%)
• IH variaza cu FiO2 direct prop. cu shuntul

Indicele de hipoxemie PaO2/FiO2
- variabilitate -
• simulare model shunt=5%, ∆PO2=0-30 kPa
• linii ingrosate – SaO2 relevante clinic (92-98%)

Indicele de hipoxemie PaO2/FiO2
- variabilitate -
6 pacienti,4 masuratori pt fiecare,2 modele –shunt si shunt+V/Q,fitting-ul modelelor la date, ∆FiO2 naste grupuri de severitate diferite la acelasi pacient;---- shunt;─ shunt + V/Q;ingrosat=SaO2 92-98%

Indicele de hipoxemie PaO2/FiO2 - grupuri de severitate la ΔFiO2 -
FiO2↓ FiO2↑
normal hO2
moderata
ALI ARDS
Shunt model Nr =23
Nr=15
Nr=40
Nr=38
Normal =64 23 14 27 0
hO2 mod=20 0 1 13 6
ALI=14 0 0 0 14
ARDS=18 0 0 0 18
Shunt+V/Q
mism
Nr=42 Nr=19 Nr=31 Nr=24
Normal=56 39 12 5 0
hO2 mod=19 3 6 9 1
ALI=23 0 1 16 6
ARDS=18 0 0 1 17
N – IH > 350 ; hipoxemie moderata – IH= 300 –350 ; ALI – IH=201-300 ; ARDS - IH <200

Indicele de hipoxemie PaO2/FiO2 - grupuri de severitate la ΔFiO2 -
“switch’’ de grup de severitate 50% pentru modelul “’shunt” si 38% pentru modelul biparametric
prin FiO2 (SpO2=92-98%)
- shunt model ALI=14 40
- shunt model ARDS=18 38
- model biparametric ALI 23 31
- model biparametric ARDS 18 24
modelul monoparametric ( shunt model ) este clar insuficient
PaO2/FiO2 depinde si de FiO2 ( calcularea IH se face
obligatoriu la acelasi FiO2 )
PaO2/FiO2 este cel putin insuficient in urmarirea ALI/ARDS

“Perhaps more appropriate would be to replace the PaO2/FiO2 ratio with two parameters, a parameter to describe the oxygenation problems due to V/Q mismatch and one to describe oxygenation problems due to shunt.”
Kjaergaard, Rees
2007,Critical Care

Key messages
ALI/ARDS – criterii de diagnostic – focus pe contextul
clinic. Protective ventilation este dictata NU de cifre ci de un context clinic.
Modelele monoparametrice vor fi interpretate avand in permanenta vedere neajunsurile si capcanele lor.
Modelele biparametrice, in lipsa ALPE, pot fi folosite la patul bolnavului sub o forma grafica. Este posibila construirea unor familii de curbe in dinamica pentru fiecare pacient. Ele descriu schimburile gazoase mai corect.